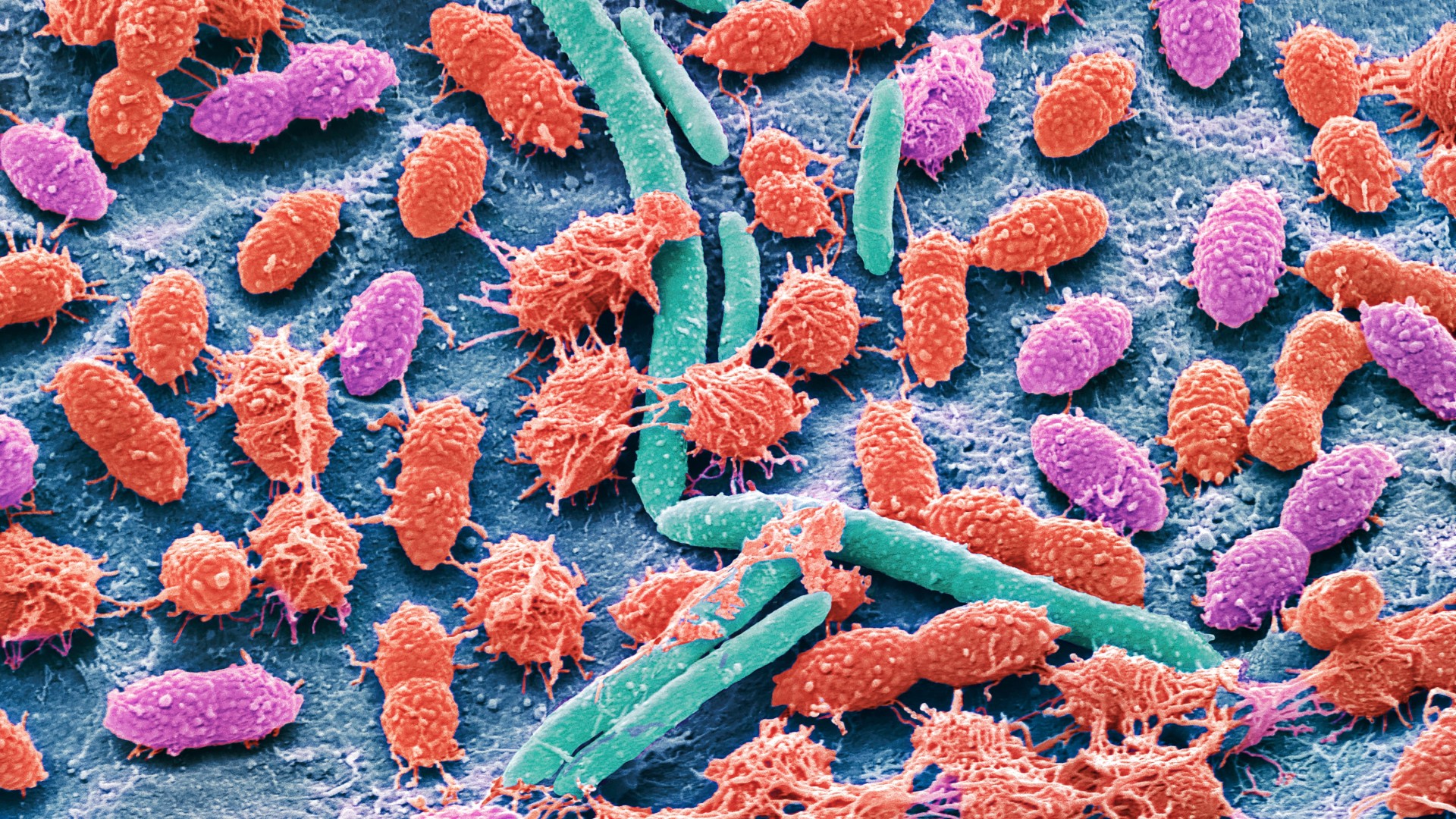
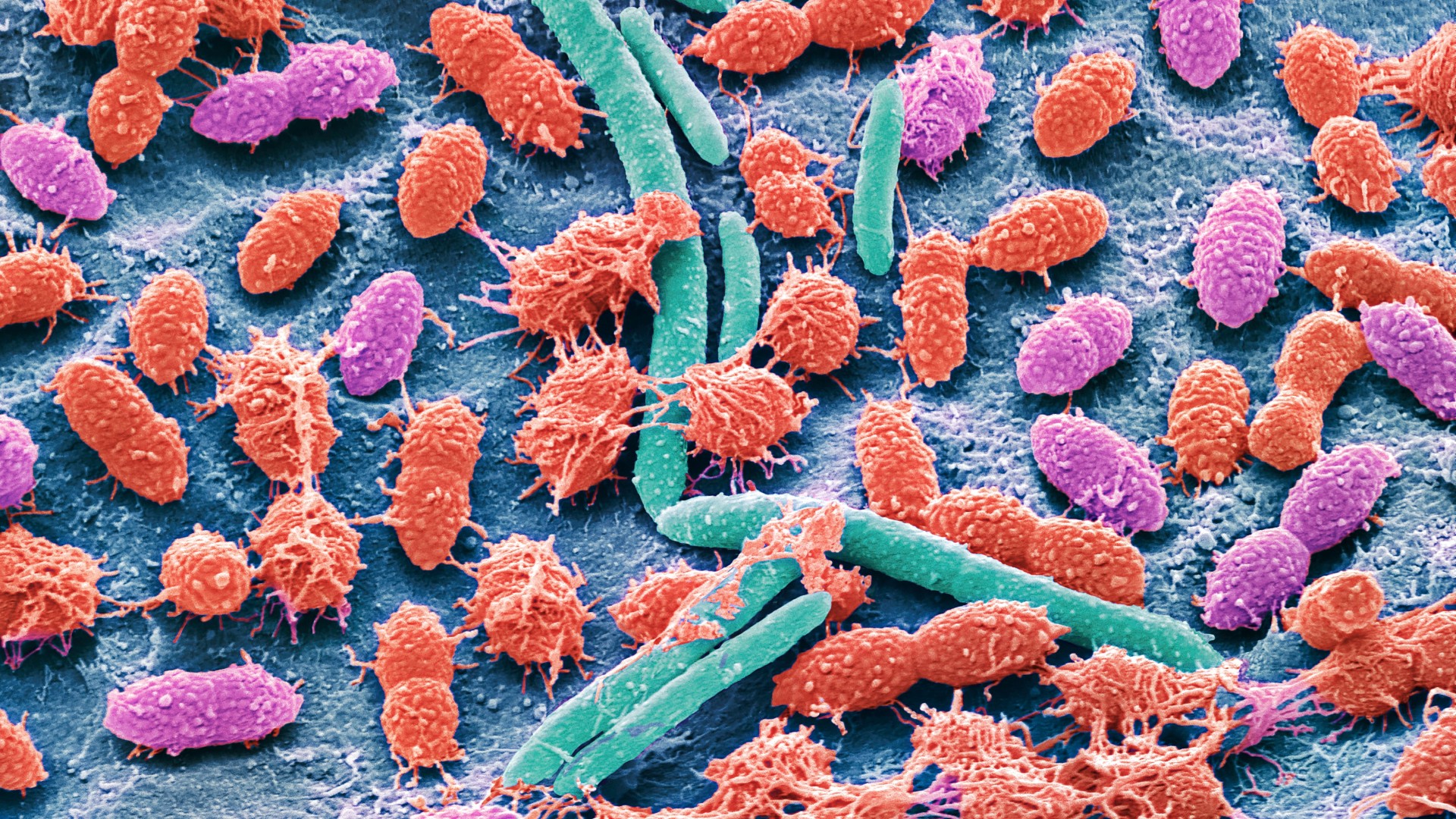
Le microbiome intestinal, cette communauté de micro-organismes résidant dans le côlon, pourrait influencer le risque d’une personne de développer des maladies chroniques, telles que le diabète de type 2 et les maladies cardiaques. Récemment, des chercheurs ont mis au point un outil informatique capable d’évaluer la « santé » du microbiome intestinal d’un individu à partir d’un simple échantillon de selles.
Bien que cette idée soit prometteuse, des experts ont exprimé des doutes quant à l’utilité réelle de cet outil pour les patients.
Appelé Gut Microbiome Wellness Index 2 (GMWI2), cet outil attribue aux utilisateurs un score variant de -6 à +6. Plus le score est élevé, plus le microbiome intestinal est considéré comme « sain ». Une étude récente, publiée le 28 août dans la revue Nature Communications, a révélé que le GMWI2 était capable de distinguer avec 80 % de précision un microbiome intestinal « sain » d’un « non sain ». Cet outil a été formé à partir d’échantillons de selles de 8 000 personnes et testé sur 1 140 échantillons.
Bien que GMWI2 soit accessible en téléchargement gratuit, une connaissance de base en informatique ou en bioinformatique est nécessaire pour interpréter les résultats, a précisé Jaeyun Sung, co-auteur de l’étude et professeur assistant de chirurgie à la Mayo Clinic dans le Minnesota.
Qu’est-ce qu’un microbiome « sain » ?
Le GMWI2 repose sur un type d’apprentissage automatique, un outil d’intelligence artificielle (IA) capable de faire des prédictions à partir de données en suivant un ensemble de règles préétabli. Les scientifiques « forment » généralement l’IA en lui fournissant de grandes quantités de données provenant d’une population donnée, puis, une fois qu’elle a identifié des motifs communs, l’outil peut faire des prédictions sur de nouvelles données provenant d’un groupe différent.
Dans ce cas, les chercheurs ont entraîné le GMWI2 à identifier des caractéristiques spécifiques des microbiomes intestinaux de personnes atteintes de maladies, comme le diabète, et à les comparer à ceux de personnes en bonne santé. Ils ont alimenté l’outil avec des données sur la composition microbienne des échantillons de selles de 8 000 personnes issues de 26 pays sur six continents.
Environ 5 500 de ces individus avaient été diagnostiqués avec l’une des 11 maladies, y compris le cancer colorectal et la maladie inflammatoire de l’intestin, comme la maladie de Crohn. Les 2 500 autres n’avaient pas de diagnostic parmi ces conditions. Après avoir formé l’outil avec ces données, les chercheurs ont testé son efficacité sur 1 140 échantillons de selles de patients atteints de maladies, telles que le cancer du pancréas et la maladie de Parkinson, ou non.
Les résultats ont montré que plus le score GMWI2 d’une personne est élevé, plus son microbiome intestinal ressemble à celui d’une personne sans maladie. Un score plus bas indique que le microbiome intestinal est distinct de celui d’un individu atteint de l’une de ces conditions.
Contrairement aux outils de diagnostic bien établis, comme les coloscopies pour le cancer colorectal, le GMWI2 n’est pas conçu pour diagnostiquer des maladies spécifiques. Il vise plutôt à signaler des changements subtils dans la santé intestinale d’une personne qui pourraient indiquer un risque accru de développer une maladie.
Au lieu de fournir des diagnostics, Sung a suggéré que cet outil pourrait être utilisé par des personnes en bonne santé souhaitant optimiser leur santé intestinale pour prévenir des maladies. Il pourrait également être bénéfique pour ceux ayant des antécédents familiaux de certaines maladies.
Le GMWI2 pourrait également servir à évaluer la récupération du microbiome intestinal après des traitements comme la chimiothérapie ou les antibiotiques, qui peuvent nuire à la flore intestinale. Ces changements induits par les traitements peuvent affaiblir le système immunitaire, rendant les patients plus vulnérables aux infections futures.
Pas de solution universelle
Malgré l’attrait potentiel d’un outil comme le GMWI2, des experts ont exprimé des réserves quant à son utilisation dans la pratique.
Cette étude représente une « tentative héroïque » de relier des signatures spécifiques du microbiome intestinal à la santé ou à la maladie, a déclaré Willem De Vos, professeur émérite de microbiomique humaine à l’Université d’Helsinki, qui n’a pas participé à la recherche. Cependant, « l’un des problèmes de cette approche est que la santé est difficile à définir – elle est plus que l’absence de maladie », a-t-il ajouté.
Certains scientifiques soutiennent qu’il n’existe pas de définition universelle de la santé, car celle-ci est relative. La santé pour une personne ne signifie pas nécessairement la même chose pour une autre. Par exemple, deux personnes peuvent obtenir un score GMWI2 de +6, mais la composition de leur microbiome peut être complètement différente, rendant difficile la définition d’un « microbiome sain ».
La santé d’une personne évolue également au cours de sa vie, ce qui signifie que tout score de santé obtenu à partir d’un outil comme le GMWI2 deviendrait « sans signification » s’il n’est pas répété dans le temps, a déclaré le Dr Fergus Shanahan, professeur et responsable du département de médecine à l’University College Cork en Irlande. De plus, l’abondance de certains microbes dans l’intestin fluctue quotidiennement et peut être influencée par l’alimentation, le stress ou l’humeur d’une personne.
Ainsi, une personne cherchant à surveiller la santé de son microbiome intestinal après une cure d’antibiotiques, par exemple, devrait utiliser l’outil régulièrement, comme chaque semaine ou chaque mois, a précisé Sung.
De plus, plusieurs versions du GMWI2 pourraient être nécessaires pour adapter l’outil à différentes populations, a ajouté Shanahan. « Plusieurs études ont montré que la composition du microbiome varie considérablement selon les groupes ethniques, parfois de manière marquée », a-t-il déclaré. Cela peut être dû à des facteurs sociaux et environnementaux variés, y compris l’alimentation et le mode de vie.
« Ainsi, tout outil de mesure de la santé d’un individu doit être adapté à la population dans laquelle il vit », a soutenu Shanahan.
Il reste également à déterminer ce que les gens pourraient faire pour modifier un score GMWI2 « suboptimal ». Dans l’article, Sung et ses collègues mentionnent que cela pourrait inciter les gens à passer des tests de diagnostic supplémentaires ou à modifier certains aspects de leur alimentation ou de leur mode de vie. Cependant, sans connaître la maladie d’un patient, il peut être difficile de mettre en œuvre des interventions ciblées.
Les chercheurs travaillent actuellement sur la prochaine version de l’outil, qui sera connue sous le nom de Gut Microbiome Wellness Index 3. (Le GMWI2 était une mise à jour du prototype plus basique, le Gut Microbiome Wellness Index, introduit en 2020 et formé sur un nombre beaucoup plus restreint d’échantillons de selles.)
Ils visent à former la prochaine itération de l’outil en utilisant au moins 12 000 échantillons de selles provenant d’une cohorte de personnes beaucoup plus diversifiée. Ils prévoient également d’utiliser des algorithmes d’apprentissage automatique plus sophistiqués pour interpréter les données. Si l’outil obtient l’approbation réglementaire, il pourrait être commercialisé dans les deux prochaines années, a-t-il prédit.